Há muitos mitos e mal-entendidos quando se trata de microbiologia, desde a «regra dos 5 segundos» para comer alimentos que caíram no chão até a tradição geracional sobre matar um resfriado de fome e alimentar uma febre. Quando se trata de microbiologia farmacêutica e salas limpas, alguns “mitos” se tornaram arraigados e até mesmo endossados por órgãos reguladores. Por exemplo, ainda há algumas autoridades que insistem na rotação de desinfetantes para evitar o desenvolvimento de cepas bacterianas resistentes. O objetivo dos autores aqui é usar a lógica e a ciência sólida para eliminar alguns mitos microbiológicos relacionados à limpeza desinfetante de ambientes controlados.
Algumas das crenças, práticas e políticas questionáveis que encontramos estão listadas abaixo:
MITO: Dados de monitoramento ambiental (ME) são um preditor confiável de risco à qualidade do produto.
FATO: Os dados de ME microbianos viáveis geralmente refletem um instantâneo no tempo, representando uma condição transitória que pode persistir ou não. Um único ponto de dados (ou seja, uma amostra de superfície) não pode necessariamente ser extrapolado como relevante além de seus parâmetros de amostra imediatos. Os autores testemunharam simulações de processos assépticos contaminados (preenchimentos de meio) onde o ME associado estava totalmente limpo (0 UFC). Por outro lado, vimos resultados positivos para um preenchimento de meio em que os dados de ME associados mostraram contaminação anormalmente alta e várias excursões de nível de alerta e ação. A interpretação de dados de ME de salas limpas é uma prática altamente diferenciada, melhor conduzida por uma equipe bem treinada, educada e experiente.
MITO: Resíduos de desinfetantes secos em superfícies apresentam risco inerente à qualidade do medicamento.
FATO: Qualquer resíduo de superfície, sob as condições certas, pode representar um risco à qualidade. A teoria de que resíduos de desinfetantes possam abrigar microrganismos viáveis é uma ideia não comprovada e bastante contraintuitiva quando se considera as necessidades metabólicas de microrganismos viáveis. Uma abordagem baseada em risco e ciência para lidar com resíduos de desinfetantes ou qualquer outro resíduo de sala limpa é o único curso de ação aconselhável.
MITO: Pulverizar desinfetantes sobre superfícies proporciona maior cobertura e, portanto, maior eficácia, em comparação à limpeza com esfregão ou pano. FATO: A técnica é importante! Desinfetantes químicos líquidos funcionam por meio do contato direto com as membranas celulares. A pulverização pode ser eficaz se uma cobertura contígua for realizada. A ação mecânica de limpar e esfregar também traz benefícios adicionais. Comparar os dois métodos não é um exercício simples ou direto. As empresas devem considerar muitos fatores ao determinar o modo ideal de aplicação para seus processos e instalações, incluindo, entre outros: materiais de superfície e complexidade, tamanho e acessibilidade das áreas e resultados históricos de ME. Uma avaliação de risco formal pode ajudar a determinar a melhor abordagem.
MITO: Recuperações de mofo do ME de uma superfície exigem uma ação corretiva usando um agente esporicida naquela superfície.
FATO: Como observado acima, os resultados do ME são um instantâneo no tempo e geralmente refletem condições transitórias. Dado o intervalo de tempo entre a coleta da amostra e o recebimento dos resultados (normalmente de 3 a 5 dias), muitas atividades provavelmente ocorreram na área, o que torna ilógico reagir como se as condições permanecessem as mesmas. Muitas vezes, a superfície em questão já terá sido tratada com um detergente germicida com eficácia fungicida. A prevenção é melhor que a reação; uma investigação completa da origem do mofo e a prevenção de sua recorrência são abordagens melhores e embasadas na ciência.
Mito: mais é melhor
Em inúmeras visitas a instalações biofarmacêuticas e de dispositivos médicos, os autores observaram regimes complexos em vigor para desinfecção de superfícies de salas limpas, envolvendo 3 ou mais variedades de desinfetantes e vários tipos de agentes esporicidas. Por exemplo, diversas empresas que visitamos recentemente na América do Sul estão implantando esses esquemas complexos. Essas abordagens complicadas para a desinfecção de salas limpas tornam o processo trabalhoso para os funcionários que executam as tarefas, sem benefícios adicionais em termos de controle de carga biológica. O fato é que o uso rotineiro de um único detergente germicida de amplo espectro, juntamente com o uso periódico e direcionado de um agente esporicida, é um programa totalmente eficaz para atingir o controle suficiente da carga biológica na grande maioria dos ambientes de salas limpas1.
P: Se um esporicida mata tudo, não deveríamos usá-lo o tempo todo?
R: A inativação química de endósporos bacterianos requer formulações bastante agressivas, como misturas de hipoclorito de sódio ou peróxido de hidrogênio PAA (ácido peracético/acético). O uso muito frequente de esporicidas à base de oxidantes pode causar problemas de corrosão na sala limpa, bem como preocupações com exposições ao meio ambiente, saúde e segurança (EHS [environment, health and safety]). Portanto, os esporicidas devem ser usados de forma criteriosa, com frequência baseada no risco e nas recuperações históricas de ME de bactérias formadoras de endósporos.
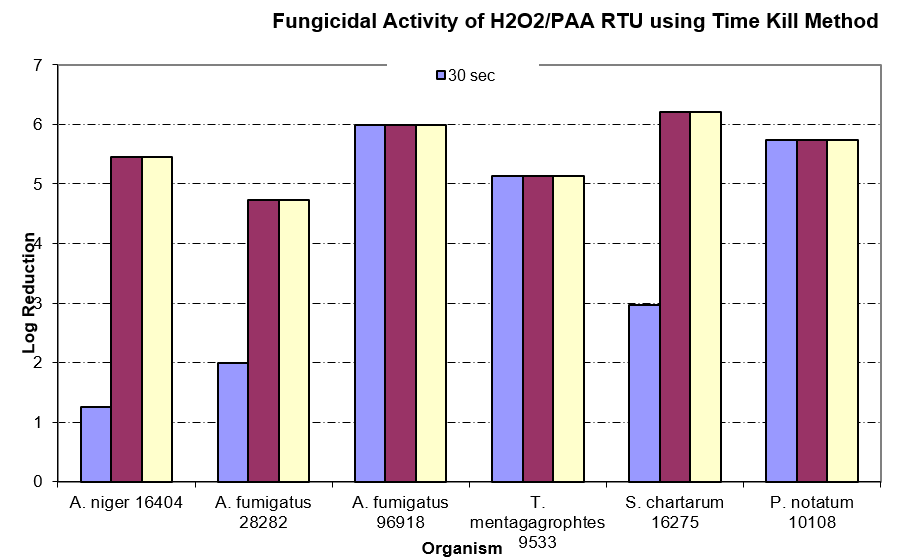
O álcool é outro agente de sala limpa que nem sempre é usado corretamente. Muitas instalações usam apenas IPA a 70% em itens que serão passados para o ambiente da sala limpa, presumindo que seja eficaz contra esporos de fungos e bactérias. Pode haver algum efeito sobre os esporos de fungos, conforme visto na tabela abaixo (estudo Time-Kill2), mas um verdadeiro agente esporicida é necessário para evitar a entrada de formadores de esporos na sala limpa
Eficácia do H2O2 / PAA RTU contra fungos
Muitas vezes, os operadores são treinados de acordo com o procedimento operacional padrão (POP) para usar movimentos sobrepostos unidirecionais com esfregões de cabeça plana em paredes e pisos. No entanto, essa técnica pode se deteriorar se a formação for insuficiente e as práticas não forem aplicadas. A preparação de diluições de uso corretas é outro elemento-chave para uma desinfecção eficaz3. Provetas graduadas e pacotes de dose unitária são a maneira mais precisa. Nunca é aconselhável despejar desinfetante concentrado em um balde usando o método do “globo ocular”.
Um programa eficaz de limpeza e desinfecção deve sempre ter um desinfetante com eficácia de amplo espectro e um esporicida para tratar endósporos bacterianos em operações de salas limpas.

(Image Credit: http://www.pppmag.com/article/714/June_2010/Cleaning_Practices_for_Cleanroom_Contamination_Control/)
Mito: os resíduos de desinfetantes acumularão biocarga e interferirão na eficácia do esporicida
A aplicação rotineira de agentes desinfetantes e esporicidas é necessária para manter o controle ambiental das salas limpas. O uso rotineiro desses produtos pode deixar resíduos na superfície. Podem ocorrer problemas devido ao uso de produtos químicos incompatíveis em rotação, mas será que resíduos de desinfetante, por si só, promovem a contaminação microbiana? E interferem na eficácia esporicida?
Os desinfetantes fenólicos de próxima geração da STERIS foram testados como resíduos em um estudo de tempo de eliminação para avaliar o impacto na eficácia de um agente esporicida (SporKlenz® RTU) vs. Bacillus subtilis, ATCC# 19659. Os sólidos (µg/cm2) do desinfetante seco foram determinados em um estudo separado, onde a quantidade de resíduo foi calculada após várias aplicações em um corpo de prova de aço inoxidável de 116 cm2 para imitar o uso típico em sala limpa, bem como a quantidade de SporKlenz RTU para cobrir uma superfície em aplicações típicas como diluente. No caso deste último, determinou-se que 120 mg de esterilizante SporKlenz RTU cobriam um corpo de prova de 116 cm2. As proporções determinadas neste experimento foram extrapoladas para determinar a diluição do resíduo desinfetante para adicionar em uma solução de agente esporicida.
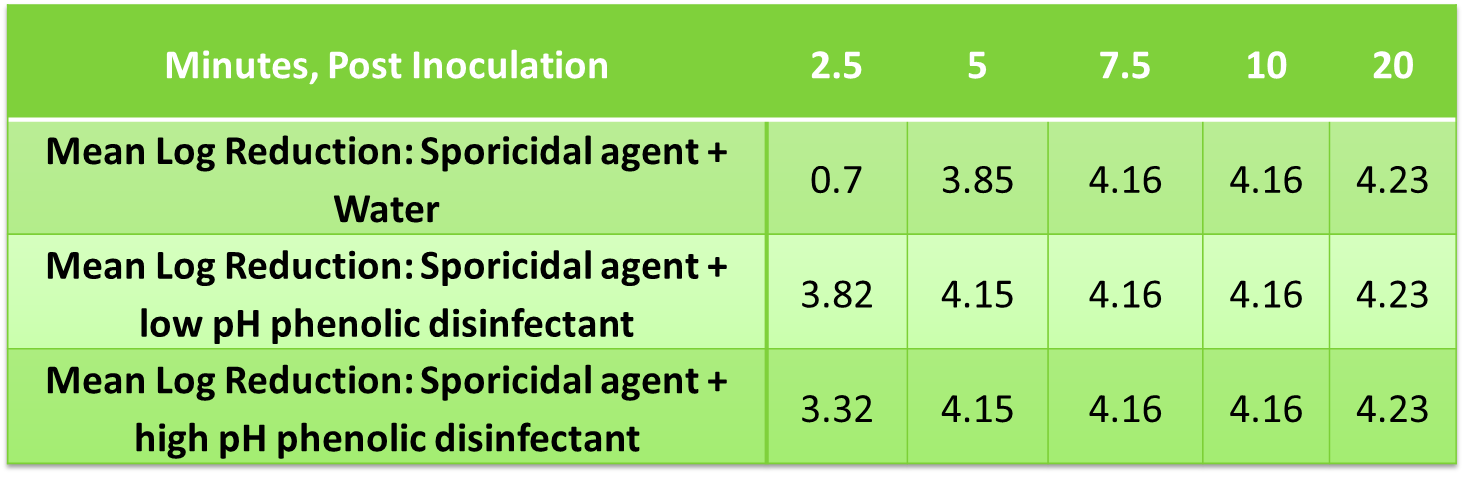
Um volume de 0,1 mL de suspensão de microrganismos foi adicionado a 9,9 mL de solução de teste (ou seja, esterilizante Spor-Klenz RTU enriquecido com um desinfetante fenólico de pH baixo ou alto). Um controle de tampão foi adicionado usando a mesma quantidade. Após a inoculação, uma amostra de 0,1 mL foi removida em 2,5, 5, 7,5, 10 e 20 minutos. As amostras foram neutralizadas, plaqueadas e incubadas por 48-49 horas a 37±2 °C. Os organismos viáveis por mL de amostra foram determinados por contagem padrão em placa aeróbica.
Redução de log médio de B. subtilis usando resíduos fenólicos e solução de agente esporicida
Da mesma forma, resíduos de desinfetantes secos foram avaliados para determinar o impacto na eficácia esporicida, uma vez que isso reflete práticas típicas de salas limpas. As amostras foram preparadas para representar 20 dias de aplicação de desinfetante em uma área conhecida, deixadas para secar e então tratadas com um volume de agente esporicida suficiente para cobrir a área conhecida ou 8,6 µL/cm2. O inóculo foi preparado a partir de uma suspensão de esporos de Bacillus subtilis, ATCC# 19659. A suspensão de esporos de teste foi diluída com água deionizada para aproximadamente 3,0 x 108 UFC/mL. A suspensão foi adicionada a tubos contendo amostras de teste ou tampão Butterfields para fornecer uma mistura de 1% v/v de microrganismo no produto de teste ou tampão. Em vários momentos, as amostras foram neutralizadas, plaqueadas e incubadas por 48 a 50 horas a 37 ± 2 °C após o inóculo. Os organismos viáveis por mL de amostra foram determinados pela contagem padrão de placas aeróbicas e transformados em valores de log 10 para análise.
Redução do log médio de B. subtilis usando resíduos fenólicos secos e solução de agente esporicida
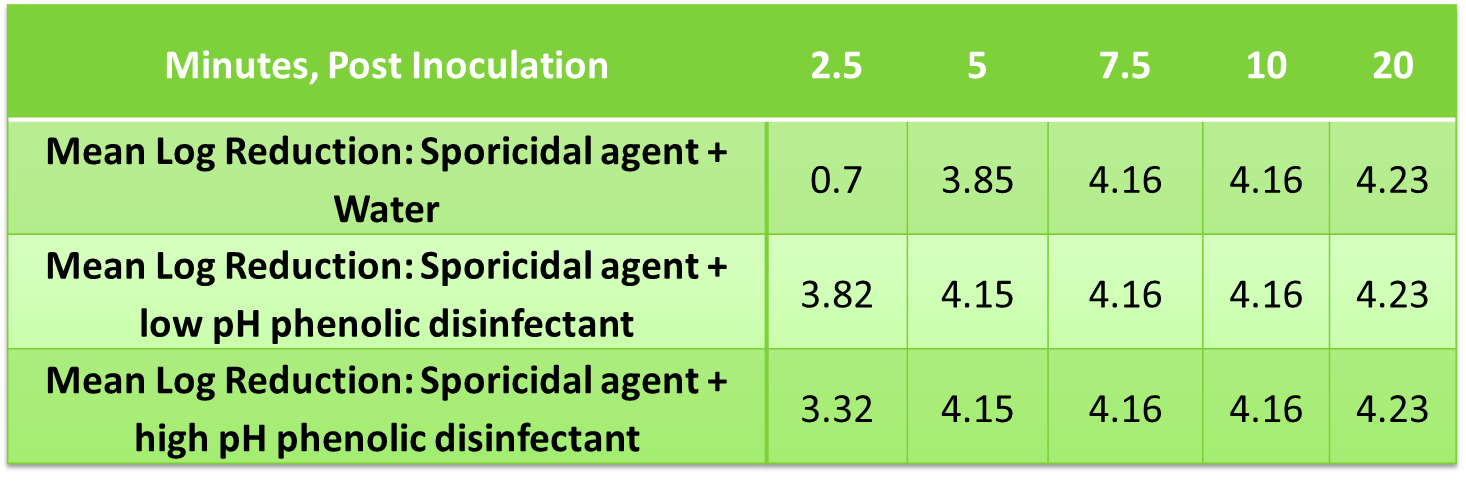
Os dados não mostram efeitos inibitórios/antagonísticos do resíduo seco com eficácia esporicida.
Formação básica
É um fato lamentável nos setores biofarmacêuticos, OSD e de dispositivos médicos que as “equipes de limpeza”, aquelas responsáveis pela limpeza desinfetante de áreas de produção de salas limpas regulamentadas, geralmente recebam a menor quantidade de treinamento, orientação e supervisão em comparação a outros departamentos (por exemplo, controle de qualidade, produção). Muitas vezes, visando economia de custos, a função de limpeza desinfetante é relegada a uma empresa de limpeza contratada, complicando ainda mais as questões de formação e removendo a equipe de limpeza da supervisão de CQ e GQ. Os horários fora de turno obscurecem ainda mais o que está acontecendo na fábrica. No mercado global de hoje, também pode haver barreiras linguísticas a serem superadas. Para complicar ainda mais as coisas, a desinfecção bem-sucedida de superfícies e ambientes de salas limpas depende totalmente das habilidades e técnicas do operador. Ao contrário da limpeza física da sujidade visível, as superfícies de salas limpas geralmente já parecem limpas. Os funcionários são então encarregados de remover a matéria não visível, seja biocarga viável ou contaminação de partículas subvisíveis. Há pouca ou nenhuma indicação visual de quando uma superfície foi efetivamente descontaminada. É por essas razões que os operadores que realizam a limpeza com desinfetantes devem ser excepcionalmente bem treinados e versados em princípios de microbiologia, controle de contaminação e práticas assépticas.
Referências:
PDA Technical Report No. 70 (2015). Fundamentals of Cleaning and Disinfection Programs for Aseptic Manufacturing Facilities. Disponível na Parenteral Drug Association, Inc.
Polarine, J., Macauley, J., Karanja, P., Klein, D., Martin, A. (2009) Evaluating the Activity of Disinfectants Against Fungi. Cleanrooms: The Magazine of Contamination Control Technology 23(2).
http://www.pppmag.com/article/714/June_2010/Cleaning_Practices_for_Cleanroom_Contamination_Control/
Ao clicar em Inscrever-se, você confirma que concorda com nossos Termos e Condições.